最近,相信不少讀者已經(jīng)被120萬元一針的CAR-T細胞治療產(chǎn)品治愈一名彌漫大B細胞淋巴瘤患者的案例刷屏了��。“120萬元治愈”和“CAR-T細胞治療產(chǎn)品”這兩個詞像井噴一樣被報道����,同時讓百姓們看到了細胞治療腫瘤的希望之余�����,也對這個價格望而卻步�。那么我們先來好好了解一下CAR-T細胞治療產(chǎn)品到底是什么來頭����?為什么價格如此昂貴?
CAR-T細胞的全稱是嵌合抗原受體T細胞(Chimeric antigen receptor T cell)�,縮寫即為CAR T cells�,翻譯過來就是CAR-T細胞。CAR-T細胞是一種基因改造后的自體T細胞�,通過基因改造技術(shù)將特定抗原受體的基因整合到T細胞內(nèi),從而使T細胞表面產(chǎn)生嵌合抗原受體����,得到嵌合抗原受體T細胞。下圖就是CAR-T細胞治療的過程�����,可以看出T細胞來自患者自體血液,通過基因改造技術(shù)得到嵌合抗原受體T細胞(c即為嵌合抗原受體)�����,最后將得到的CAR-T細胞輸回患者體內(nèi)���。
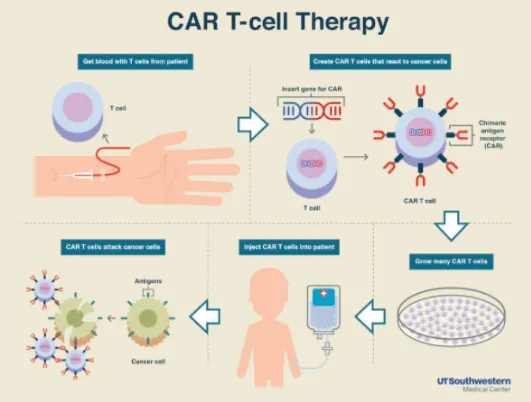
嵌合抗原受體(CAR)是什么�����?
想必不少讀者看到這里�����,大概明白了CAR-T細胞到底是什么細胞�,但是對這個“嵌合抗原受體”還是有些迷糊。為什么叫嵌合呢���?這里的嵌合抗原受體就是CAR-T細胞表面的一圈具有抗原識別功能的小“十字架”(上圖中的c)�����,本質(zhì)仍是一種蛋白質(zhì)����。而嵌合的意思就是因為這種受體不僅具有原T細胞的活化功能,同時還具有新的抗原識別功能�����。因此CAR-T細胞療法就是CAR-T細胞在進入患者體內(nèi)后����,其細胞表面的嵌合抗原受體識別體內(nèi)的癌細胞�,從而對癌細胞進行攻擊達到治療目的。嵌合抗原受體的另一個重要作用����,讓CAR-T細胞只識別攻擊癌細胞的表面抗原,而不會誤傷健康細胞��。
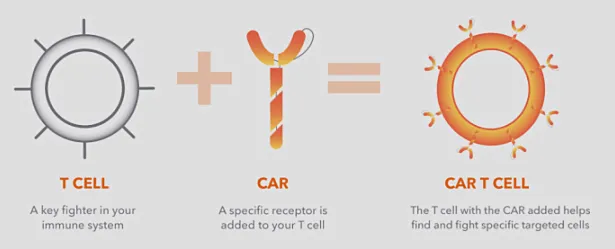
嵌合抗原受體(CAR)是如何產(chǎn)生的
那么嵌合抗原受體是如何產(chǎn)生的呢?T細胞經(jīng)歷了什么改造呢����?這里就涉及到了很重要的一步——基因改造。T細胞從患者體內(nèi)血液收集得到后�����,會在體外接受刺激擴增��,并通過病毒載體轉(zhuǎn)染特定的基因�����,成為CAR-T細胞���?;蚋脑旒夹g(shù)環(huán)節(jié)需要通過病毒載體�,因此最后得到的CAR-T細胞產(chǎn)品有可能會出現(xiàn)微生物安全性的問題,例如外源病毒因子污染���、載體來源復制型病毒(RCR/RCL)的產(chǎn)生等��。
我國的食品藥品檢定研究院在2018年6月5日發(fā)布了《CAR-T細胞治療產(chǎn)品質(zhì)量控制檢測研究及非臨床研究考慮要點》����,其中就轉(zhuǎn)染T細胞的病毒載體的純化及濃縮工藝、質(zhì)量控制檢測及如何保存等進行了規(guī)定����。由此可見,CAR-T細胞的制備工藝中所使用的病毒載體�,其生物安全性及制備保存等均有一定難度。

非病毒載體制備CAR-T技術(shù)
CAR-T治療的成本高價格貴是老百姓一直關(guān)注的問題,之所以價格貴是因為制劑生產(chǎn)時所必需的病毒載體和質(zhì)粒等重要原料均為國外采購��。所以����,使最終成藥本地化、國產(chǎn)化�,才不能被“卡脖子”�����。為了減少CAR-T細胞制備過程中的工藝難度�,國內(nèi)已經(jīng)將目標盯準了非病毒載體并取得了一定收獲��。
2019年���,我國的科學家錢其軍教授團隊研發(fā)的非病毒載體?CD19 CAR-T細胞注射液(BZ019)榮獲該年度的“中國醫(yī)藥生物技術(shù)十大進展”�。錢其軍指出�����,這種以非病毒載體體系制備得到的CAR-T細胞治療產(chǎn)品��,在安全性��、有效性和成本方面相比較于病毒載體體系均具有一定優(yōu)勢���。此項CAR-T細胞治療產(chǎn)品已獲得藥監(jiān)局許可�����,并已啟動臨床項目計劃���。
目前世界各地正在進行500多項臨床試驗�,研究可用于癌癥治療的CAR-T細胞�����,以擴大CAR-T細胞的準確性和療效��。美國佐治亞理工學院的Gabe Kwong教授團隊發(fā)現(xiàn)熱量刺激CAR-T細胞可以破壞腫瘤并防止復發(fā)����。此項研究已經(jīng)發(fā)表在《Nature Biomedical Engineering》上。
此項研究中Gabe Kwong教授團隊將激光脈沖在小鼠體外發(fā)射到腫瘤所在的地方�,小鼠體內(nèi)腫瘤處的金納米棒會將光波轉(zhuǎn)化為局部較為溫和的熱量,將局部溫度提高到40-42攝氏度����。此溫度剛好可以激活T細胞的開關(guān)�����,同時不會過熱損害健康組織或T細胞�。研究發(fā)現(xiàn)激光脈沖一旦開啟后,T細胞隨即激活,開始表達相關(guān)的抗癌蛋白質(zhì)�����。研究結(jié)果表明��,熱控CAR-T細胞治愈了小鼠模型的癌癥���,此方法不僅縮小了腫瘤���,還防止了復發(fā)。
此項研究的創(chuàng)新之處在于腫瘤內(nèi)CAR-T細胞的活動可以通過安插在細胞內(nèi)的相關(guān)基因進行光熱控制���,這些基因開關(guān)會觸發(fā)其他基因的表達�����,以應(yīng)對溫度升高(40-40°C)����,這是團隊過去三年來一直在努力的�����。Gabe Kwong教授表示他們未來將使用聚焦超聲波進行熱控研究,因為聚焦超聲波完全無創(chuàng)�����,可以針對體內(nèi)的任何部位��。激光的局限性之一是穿透身體能力有限�����,對于體內(nèi)的深層惡性腫瘤使用此方法可能會受限����。
Gabe Kwong教授說除了一個對熱量做出反應(yīng)的基因開關(guān)外,他們的研究團隊還對T細胞進行了一些升級���,可以精確控制細胞內(nèi)的工程蛋白質(zhì)(細胞因子和雙特異性T細胞參與者)的生產(chǎn)以刺激免疫系統(tǒng)���。

目前����,國內(nèi)已開啟“CAR-T細胞治療元年”��,復興凱特的CAR-T細胞治療產(chǎn)品阿基侖塞注射液與藥名巨諾的靶向CD19的CAR-T細胞產(chǎn)品瑞基奧侖賽注射液均獲得國家藥監(jiān)局批準上市�。相信不久之后,會有第三個�、第四個…第n個患者接受CAR-T細胞療法后治愈,“120萬”的天價藥物隨著工藝技術(shù)的迭代也會降下來���,可以讓更多普通百姓也能“看得起病�����,用得起藥”�����!