慢性疼痛是一個(gè)常見的臨床問題����。據(jù)多年前的估計(jì)�,慢性疼痛影響著世界上高達(dá)30%的成年人。2014年美國疼痛協(xié)會報(bào)道慢性疼痛每年給美國經(jīng)濟(jì)造成超過6000億美元的醫(yī)療支出���、殘疾補(bǔ)償和生產(chǎn)力損失���。藥物、按摩�����、針灸�、電刺激、神經(jīng)阻滯和手術(shù)都是治療慢性疼痛的傳統(tǒng)療法���。這些方法對某些患者來說可能是有效的�����。然而����,目前還沒有完全和明確的方法能完全治愈疼痛�。
干細(xì)胞療法是一種新的治療常見慢性疼痛的方法。間充質(zhì)干細(xì)胞 (MSCs)既可以替代丟失和損傷的細(xì)胞�����,同時(shí)可作為各種營養(yǎng)因子的運(yùn)載工具 �����。
間充質(zhì)干細(xì)胞(MSCs)可從人類胚胎或成人組織中衍生��,也可從成熟細(xì)胞中創(chuàng)造��,與骨髓�、骨骼肌和臍帶血等來源相比,脂肪組織可以作為MSCs的大型資源庫 �。近年來,各生物醫(yī)學(xué)研究領(lǐng)域都對干細(xì)胞治療有極大興趣 ����。
血液疾病����、燒傷�����、骨髓移植�����、角膜移植都是使用干細(xì)胞治療的例子�。干細(xì)胞可以提供治療疼痛的方法,如治療骨和軟骨缺陷�����、骨關(guān)節(jié)炎��、肌腱和韌帶損傷����,甚至是神經(jīng)損傷 ,雖然現(xiàn)在下結(jié)論還為時(shí)過早�,但可能該療法不僅能控制癥狀,還能治療原發(fā)病 。此外��,人類和動物的研究都己確定MSCs的安全性��。
近年來�����,有大量的研究工作和資金用于研究MSCs治療疼痛疾病 �。但目前��,尚無系統(tǒng)的�����、有臨床針對性研究證實(shí)干細(xì)胞療法的優(yōu)勢��。本文希望對目前的研究和臨床試驗(yàn)進(jìn)行整理��,以評估干細(xì)胞療法治療慢性疼痛的安全性���、有效性和適用性�����。以下介紹干細(xì)胞療法的臨床研 究用于治療幾種常見的慢性疼痛病�����。
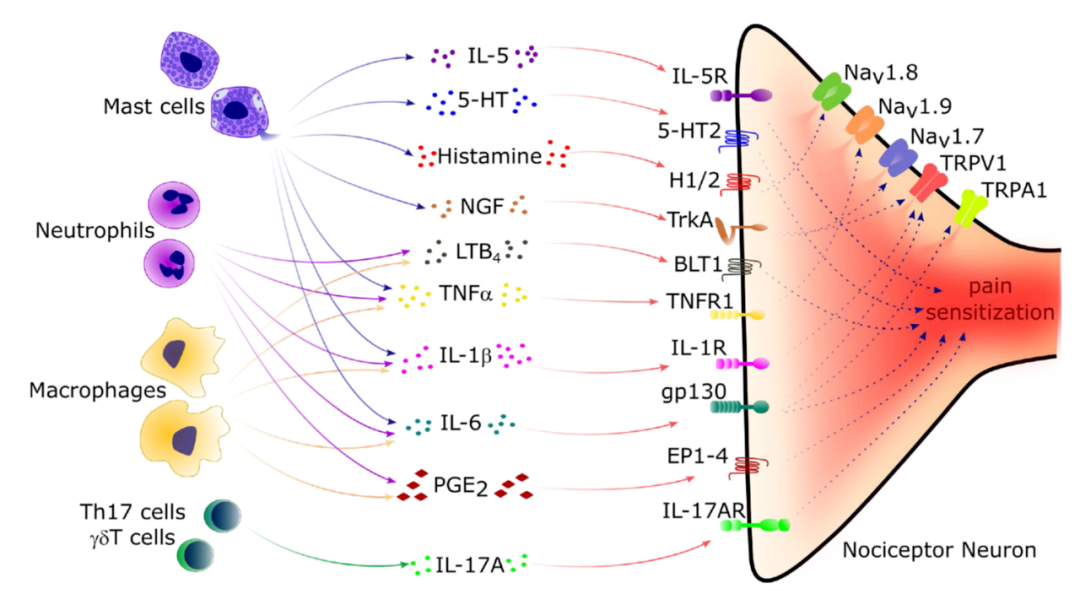
首先我們要知道�����,疼痛是炎癥的主要特征之一�����。組織損傷后局部釋放的炎癥介質(zhì)--包括經(jīng)典介質(zhì)(如緩激肽���、前列腺素���、組織胺、ATP��、神經(jīng)生長因子)、促炎細(xì)胞因子和趨化因子以及新興介質(zhì)(比如細(xì)菌N-甲?;暮蚼icroRNA)可以直接刺激和敏感化位于周圍組織初級傳入神經(jīng)元神經(jīng)纖維上的痛覺感受器。
免疫系統(tǒng)和神經(jīng)系統(tǒng)之間的雙向信號決定了慢性疼痛的發(fā)生和維持����。神經(jīng)炎癥是由于周圍神經(jīng)系統(tǒng)中的神經(jīng)膠質(zhì)細(xì)胞、中樞神經(jīng)系統(tǒng)中的小膠質(zhì)細(xì)胞��、星形膠質(zhì)細(xì)胞和少突膠質(zhì)細(xì)胞的激活����,以及包括常駐肥大細(xì)胞和巨噬細(xì)胞在內(nèi)的免疫細(xì)胞的激活以及中性粒細(xì)胞和T細(xì)胞的浸潤引起的。在外周����,白細(xì)胞介素-1β����、腫瘤壞死因子α、緩激肽���、P物質(zhì)��、降鈣素基因相關(guān)肽�、神經(jīng)生長因子和前列腺素等炎癥環(huán)境由常駐和浸潤的免疫細(xì)胞以及感覺神經(jīng)末梢釋放。簡而言之����,炎癥因子刺激神經(jīng)細(xì)胞產(chǎn)生疼痛感覺。
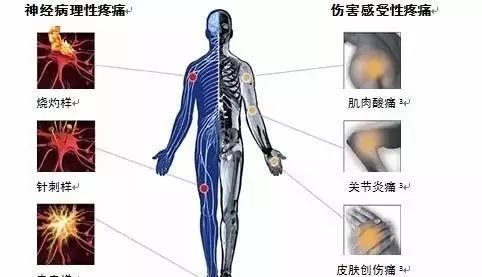
常見的疼痛包括神經(jīng)和脊髓損傷引起的神經(jīng)病理性疼痛、關(guān)節(jié)炎引起的炎性疼痛�����、癌癥疼痛和藥物治療引起的疼痛�。MSC作為治療傳統(tǒng)藥物無效的嚴(yán)重骨關(guān)節(jié)炎、神經(jīng)性疼痛和頑固性肌肉骨骼疼痛的一種替代或有前途的方法����,已被頻繁地應(yīng)用于疼痛的治療。
神經(jīng)病理性疼痛
不同于盤源性腰痛�,神經(jīng)病理性疼痛有多種臨床類型,包括三叉神經(jīng)痛 ���、糖尿病性神經(jīng)病變等 �。
骨髓間充質(zhì)干細(xì)胞(BM-MSC)具有免疫調(diào)節(jié)作用 �����,在治療時(shí)可能有助于減少神經(jīng)炎癥反應(yīng)和免疫介導(dǎo)的損傷��。從理論上講�,MSCs早期移植可能通過多種機(jī)制改善和恢復(fù)功能���,包括調(diào)節(jié)炎癥因子的產(chǎn)生��、抑制神經(jīng)膠質(zhì)增生��、通過血管生成作用促進(jìn)脊髓的血運(yùn)重建和刺激生物活性分子及生長因子的產(chǎn)生。

有研究者用脂肪來源的MSCs注射至受影響的三叉神經(jīng)����,8例藥物治療失敗的面部神經(jīng)性疼痛病人的平均疼痛評分均有下降,且無嚴(yán)重并發(fā)癥��;Venturi等人用自體脂肪組織衍生的干細(xì)胞治療常規(guī)藥物治療無效的陰部神經(jīng)痛,大部分病人疼痛評分顯著下降��,總體功能有所改善��,無不良事件報(bào)告�����。盡管這些研究取得了很好的結(jié)果��,但他們都是小樣本���、非隨機(jī)�����、非對照研究�����,而且雖然前一項(xiàng)研究試圖分離MSCs�����,但后者涉及直接注入含有異質(zhì)細(xì)胞的脂肪組織提取物����,這使得特定細(xì)胞和鎮(zhèn)痛反應(yīng)之間的聯(lián)系非常困難。然而�,由于治療神經(jīng)病理性疼痛十分困難,現(xiàn)有治療都存在局限性��,對于傳統(tǒng)治療反應(yīng)不佳的病人����,干細(xì)胞治療仍是可嘗試的。
膝骨關(guān)節(jié)炎
滑膜中白細(xì)胞介素-6(IL-6)和腫瘤壞死因子-α(TNF-α)的升高以及股外側(cè)肌中TNF-α和IL-1β的升高都與骨性關(guān)節(jié)炎患者的疼痛和肌肉萎縮密切相關(guān)��。MSC可以通過控制炎癥�����、減少軟骨丟失和提高軟骨含量來減緩膝骨關(guān)節(jié)炎的進(jìn)展����。越來越多的研究表明,MSC的主要益處來自旁分泌活動��。
?
接受經(jīng)皮關(guān)節(jié)內(nèi)注射自體MSC的患者�����,注射24周后����,患者在MRI上有統(tǒng)計(jì)學(xué)意義的軟骨和半月板生長,活動范圍增加���,改良VAS疼痛評分降低�,疼痛評分從4/10顯著下降到0.38/10�。
?

不同劑量的MSC關(guān)節(jié)腔注射�,都能做到6個(gè)月后所有劑量的患者WOMAC功能評分和疼痛評分都有下降,但是低劑量組患者的病情有反復(fù)的趨勢��。而且關(guān)節(jié)腔內(nèi)注射高劑量組(1.0×108)MSC�����,在注射后6個(gè)月W可見厚而透明的軟骨再生�,軟骨缺損面積縮小,膝關(guān)節(jié)功能和疼痛改善明顯�,無不良反應(yīng)。隨后���,這個(gè)韓國團(tuán)隊(duì)跟蹤這些患者2年�,發(fā)現(xiàn)只有高劑量組的臨床結(jié)果在兩年后趨于平穩(wěn),而中低劑量組的療效并不能維持2年��。
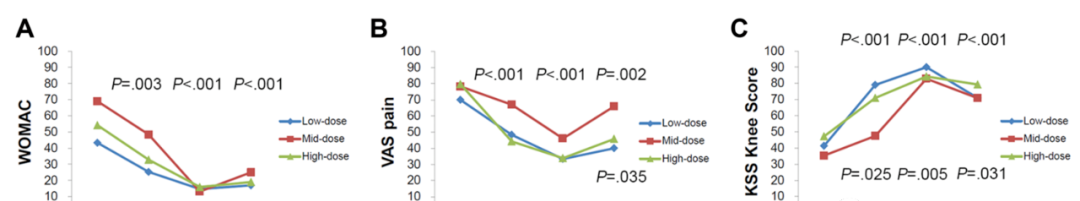
但是西班牙團(tuán)隊(duì)臨床研究發(fā)現(xiàn)不同劑量的MSC(1.0×107,1.0×108)���,單次注射1年后����,患者的膝骨關(guān)節(jié)炎病情又開始復(fù)發(fā)����。隨后這個(gè)西班牙團(tuán)隊(duì)繼續(xù)開展自體骨髓MSC聯(lián)合PRP關(guān)節(jié)腔注射治療膝骨關(guān)節(jié)炎,1年后的WOMAC評價(jià)發(fā)現(xiàn)MSC加PRP療效和單獨(dú)使用PRP的療效沒有統(tǒng)計(jì)學(xué)差異�����。注意,這只能解讀為在1年的時(shí)間點(diǎn)�,西班牙團(tuán)隊(duì)這次生產(chǎn)制備的MSC并沒有發(fā)揮很好的治療作用��,不能解讀為”MSC”沒有治療作用���。因?yàn)橥粋€(gè)團(tuán)隊(duì)的前期研究就已經(jīng)證明了MSC的療效�。
?
回顧性評估了467例(483膝)接受MSC聯(lián)合纖維蛋白膠支架植入治療膝骨性關(guān)節(jié)炎的患者�,至少隨訪5年,多因素分析顯示����,年齡越大、病情越重���,預(yù)后越差�����,MSC數(shù)量越多�,注射治療的預(yù)后越好���,但是單次的治療對影像學(xué)指標(biāo)的改善有限�。
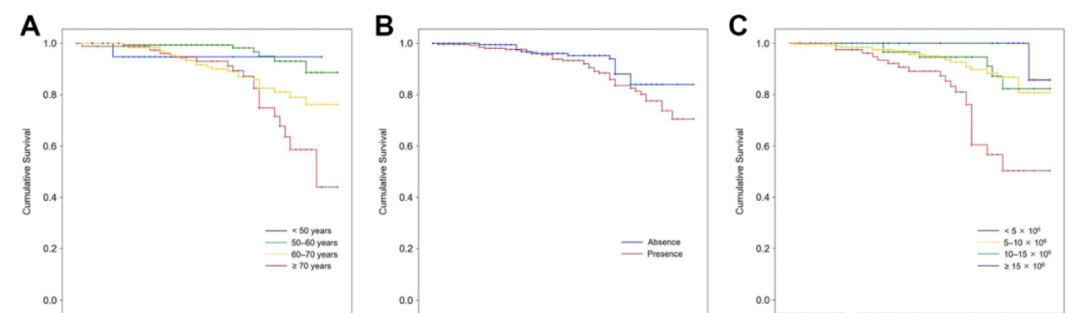
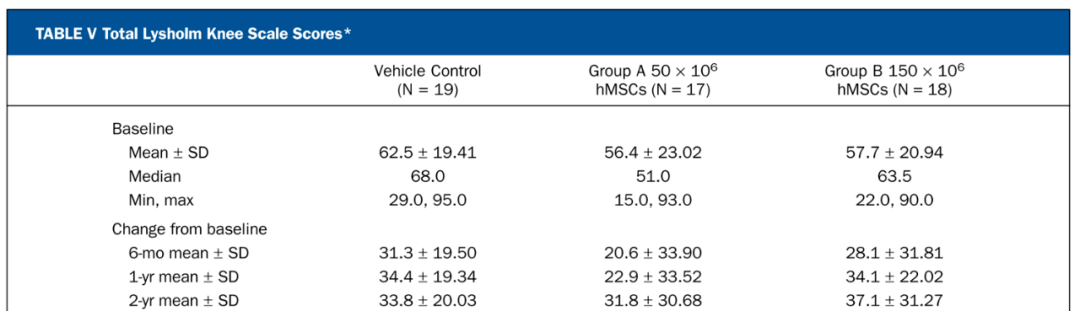
在一項(xiàng)RCT研究中�, 55名接受半月板部分切除術(shù)的患者,被隨機(jī)分成兩組����,分別在術(shù)后注射透明質(zhì)酸鈉或兩種不同劑量的同種異體骨髓間MSC(5×107,15×107)��,并對這些患者進(jìn)行了兩年多的隨訪����,MSC治療組患者的半月板體積顯著增加(預(yù)先定義為15%的閾值),疼痛顯著減輕����。
風(fēng)險(xiǎn)與潛在副反應(yīng)
在臨床上,大多數(shù)試驗(yàn)及研究報(bào)告中沒有發(fā)現(xiàn)明顯的不良事件��,但Peeters等人完成了844個(gè)樣本和關(guān)節(jié)注射的Meta分析��,評價(jià)8種涉及自體MSCs的不同研究���,共發(fā)現(xiàn)4起嚴(yán)重不良事件 (1例骨髓穿刺相關(guān)感染��,1例肺栓塞�����,2例在注射部位腫瘤)����,手術(shù)并發(fā)癥22例���,7例干細(xì)胞產(chǎn)品相關(guān)的不良事件���。其他有報(bào)道的不良反應(yīng)事件均較輕微并有自限性,包括疼痛�����、腫脹�、蕁麻疹、短暫的轉(zhuǎn)氨酶升高����、抽血點(diǎn)的刺痛等。自體BMSCs的使用不會導(dǎo)致免疫反應(yīng)或疾病傳播。重要的是�,惡性腫瘤等的發(fā)生過程可能需要較長時(shí)間,這些不良后果可能存在于研究隨訪的范圍之外���,但仍有一些研究表示�����,長期體外擴(kuò)增MSCs有自發(fā)性惡性轉(zhuǎn)化的風(fēng)險(xiǎn)���。
正在進(jìn)行的干細(xì)胞療法臨床實(shí)驗(yàn)
目前正在進(jìn)行的一些臨床試驗(yàn)涉及脊柱退行性疾病、關(guān)節(jié)病�、神經(jīng)病理性疼痛和一些混合性疾病。大多數(shù)研究仍處于 I期及II期臨床試驗(yàn)����,希望這些l臨床試驗(yàn)?zāi)芙o病人提供機(jī)會,特別是對那些常規(guī)治療失敗的病人����。
本文總結(jié)了利用干細(xì)胞作為一種新的療法治療疼痛相關(guān)疾病的有效性,但將此療法應(yīng)用于臨床應(yīng)謹(jǐn)慎對待���,總之�����,我們堅(jiān)信慢性疼痛疾病的干細(xì)胞治療前景廣闊����。